Mélanges et séparation
I. Mélanges
On a un mélange lorsqu’on met au moins deux espèces ensemble et qu’on agite. Le mélange peut être hétérogène ou homogène.
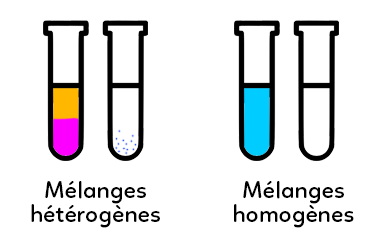
Il est hétérogène lorsqu’on voit plusieurs parties à l’œil nu. Par exemple, c’est le cas pour le mélange huile-vinaigre (vinaigrette) : l’huile est au-dessus et le vinaigre en dessous, même après agitation. De même, pour le mélange sable-eau où le sable reste au fond même après agitation. Ce sont bien deux mélanges hétérogènes.
A l’inverse, on a aussi des mélanges homogènes : après agitation on ne voit qu’une seule partie à l’œil nu. Par exemple, c’est le cas du mélange sirop-eau ou eau-sucre.
II. Séparation
On se place dans le cas d’un mélange solide-liquide. Les deux premières techniques de séparation concernent un mélange hétérogène solide-liquide et la troisième technique un mélange homogène solide-liquide.
A. La décantation
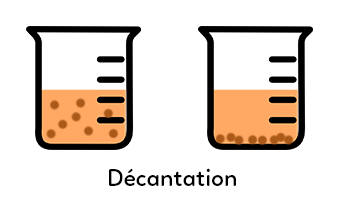
Cela signifie qu’on laisse reposer le mélange. Au départ, on agite le mélange puis on le laisse reposer un certain temps. Dans le cas d’un mélange solide-liquide, on observe que le solide tombe au fond et que le liquide surnage. C’est l’inverse si le solide flotte.
B. La filtration
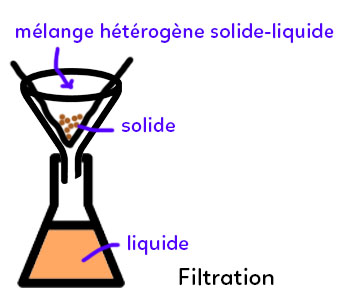
On utilise un filtre, comme pour les anciennes machines à café, que l’on va placer sur un entonnoir disposé dans un récipient appelé erlenmeyer. On va ensuite verser le mélange hétérogène dans l’entonnoir avec le filtre et le solide va rester dans le filtre tandis que le liquide sera à l’intérieur du récipient. La méthode de filtration est beaucoup plus efficace que celle de la décantation et on fait souvent une filtration après décantation.
C. L’évaporation
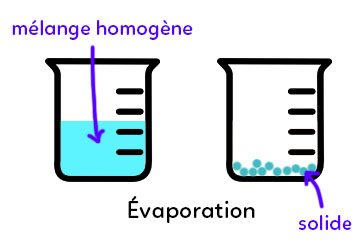
Un mélange homogène solide-liquide comme une eau sucrée ou salée peut subir une évaporation pour séparer les deux constituants du mélange. On place l’eau sucrée ou salée dans une coupelle et on la laisse à l’air libre quelques jours. L’eau va naturellement s’évaporer (d’où le nom d’évaporation) et on va récupérer le solide au fond du récipient (sucre ou sel). L’inconvénient de cette technique est que l’on récupère le solide du mélange mais pas l’eau qui s’est évaporée.


