Transferts thermiques - Changements d'état
Rappels
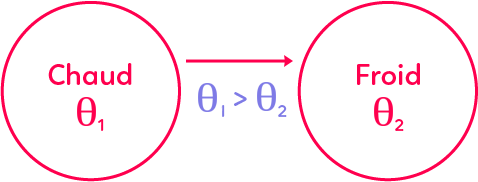
Lorsqu’un corps chaud à la température $Θ1$ est mis en contact avec un corps froid à la température $Θ2,$ il y a un échange d’énergie sous forme de transfert thermique.
Un transfert thermique peut provoquer une variation de la température du corps et/ou un changement d’état.
Changements d’état de matière
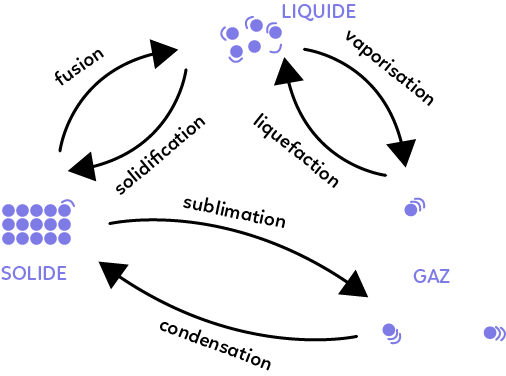
La matière existe sous trois états : l’état solide, l’état liquide et l’état gazeux. L’état solide est très organisé, l’état liquide est plus désorganisé et l’état gazeux est encore plus désorganisé que l’état liquide. Chaque rond violet représente une entité de matière comme un atome, une molécule ou un ion.
Certains changements d’état sont endothermiques, c’est-à-dire qu’ils ont besoin qu’on leur apporte de l’énergie pour se réaliser. Fusion, vaporisation et sublimation sont endothermiques, en effet on passe d’un état ordonné à un état plus désordonné, on fournit de l’énergie pour agiter les particules de matière.
D’autres changements d’état sont exothermiques, c’est-à-dire qu’ils libèrent de l’énergie à l’extérieur. Solidification, condensation et liquéfaction sont exothermiques car on passe d’un état désordonné à un état plus ordonné, on libère de l’énergie à l’extérieur.
Calcul du transfert thermique lors d’un changement d’état
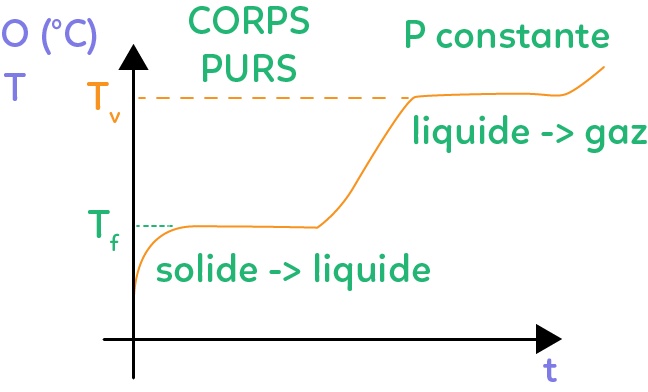
Voici le graphe de l’évolution de la température en fonction du temps lors de deux changements d’état pour un corps pur à pression constante. Supposons que l’on mette une entité à l’état de solide, on chauffe progressivement et on mesure la température en fonction du temps. Si le corps est pur et la température constante on va donc obtenir cette courbe. Au début, la température augmente, puis il y a un palier de température qui correspond au changement d’état solide-liquide. Au début le corps pur est à l’état solide, au virage de la courbe on a l’apparition de la première goutte de liquide, puis on a le palier du changement d’état solide-liquide. Il se fait à une température constante $T_f$ qu’on appelle température de fusion. Au prochain virage de la courbe, il n’y a plus de solide. On continue à chauffer la matière à l’état liquide et il y a de nouveau un palier de température. Celui-ci correspond au changement d’état liquide-gaz. On obtient la dernière goutte de liquide au virage et ensuite la matière est à l’état gazeux. Ce palier correspond à la température de vaporisation $T_v$.
Pour rappel, $T_f$ et $T_v$ caractérisent un corps pur à une pression donnée. Par exemple, si un corps fond à 0°C et se vaporise à 100°C, on sait que c’est de l’eau pure.
Donc, pour calculer le transfert thermique pendant un changement d’état, on a la relation suivante : $Q = mL$
Avec $Q$ le transfert thermique noté aussi $ΔE$ exprimé en Joules, $m$ la masse de corps utilisée en $kg$ et $L$ l’énergie massique de changement d’état exprimée en J.kg-1. Cette dernière correspond à l’énergie qu’il faut pour faire un changement d’état pour $1kg$ du corps étudié.
Les énergies massiques de changement d’état sont à l’opposé l’une de l’autre si les deux changements d’état sont opposés l’un de l’autre. Par exemple :
Lfusion = -Lsolidification
Lvaporisation = -Lliquéfaction
Lsublimation = -Lcondensation
Ces grandeurs sont fournies, il faut juste savoir utiliser la formule. Il faut aussi interpréter le signe de ces grandeurs. Le signe de $L$ est le même que celui de $Q$ puisque $m$ est positif (kg). Ainsi pour la fusion, la vaporisation et la sublimation, l’énergie massique de changement d’état est positive. Pour la solidification, la liquéfaction et la condensation, l’énergie massique de changement d’état est négative.
Changements d'états
Changements d’états
I. Quels sont les changements d’états existants ?
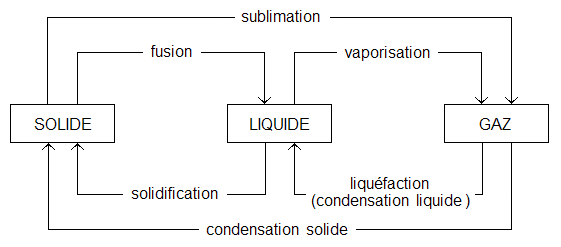
La matière existe à l’état solide, liquide ainsi que gazeux. Les changements entre ces différents états on des noms qu’il faut connaître :
Le changement d’état du solide vers le liquide est la fusion.
Le changement d’état du liquide vers le solide est la solidification.
Le changement d’état du liquide vers le gaz est la vaporisation.
Le changement d’état du gaz vers le liquide est la liquéfaction.
Le changement d’état du solide vers le gaz est la sublimation.
Le changement d’état du gaz vers le solide est la condensation.
Lorsque l’on veut écrire l’équation d’un changement d’état (fusion) pour un corps pur, par exemple de l’eau, il suffit d’écrire :
$H_2 O_{(s)} \to H_2 O_{(l)} $
II. Changements d’états endothermiques et exothermiques
D’un point de vue énergétique, certains changements d’états sont endothermiques et d’autre exothermiques :
– Un changement d’état est dit endothermique lorsque l’on doit apporter de l’énergie à la réaction. Les changements concernés sont la sublimation, la fusion et et la vaporisation
– A l’opposé un changement d’état est exothermique lorsqu’il dégage de l’énergie, cela concerne la liquéfaction, la solidification et la condensation.
III. Energie de changement d’état Q
Il existe une énergie de changement d’état notée Q qui peut se déterminer.
La formule à connaître est $Q =m \times L,$ où $Q$ s’exprime en joules (J), la masse en kilogrammes (kg) et l’énergie massique, que l’on note $L,$ en joules par kilogramme (J.kg-1).
Toutes les énergies massiques de changements d’états sont répertoriées dans une base de donnée accessible (un livre).
Exemple : la fusion de l’eau
Son énergie massique de changement d’état est $L_{fusion}(H_2O)=330 \ kJ.kg^{-1}$.
Ainsi pour faire fondre $1 \ kg$ de glace, il faut fournir $330 \ kJ$. De plus, par convention, un changement d’état endothermique possède une énergie Q positive, et pour un changement d’état exothermique Q est négative.
Pour finir, lorsque que deux changements d’états sont opposés l’un à l’autre, alors leur énergie massique de changement d’états sont opposées : $L_{fusion}=-L_{solidification}$ et $L_{vaporisation}=-L_{liquéfaction}$.