Étude à différentes échelles phénotypiques d'une maladie génétique : la drépanocytose
On étudie à différentes échelles phénotypiques une maladie génétique appelée drépanocytose ou anémie falciforme.
Le phénotype est l’ensemble des caractères observables et ces observations peuvent se faire à différentes échelles. Il existe l’échelle macroscopique (à l’œil nu) mais on peut aussi descendre à l’échelle microscopique avec un microscope optique, et même à l’échelle moléculaire avec des logiciels type Anagène et Rastop. Dans le cas de l’étude d’une maladie, il est nécessaire d’avoir un témoin. Quand on se pose une question sur une échelle (moléculaire, cellulaire ou encore macroscopique), on doit toujours comparer l’individu malade, ici de phénotype drépanocytaire, à un individu dit sain, qui n’a pas la maladie.
I. Comment les échelles phénotypiques sont-elles emboitées ?
Il s’agit d’une maladie génétique, donc on commence par les gènes : l’échelle moléculaire. En cours, quand on étudie les gènes, on travaille sur le logiciel Anagène.
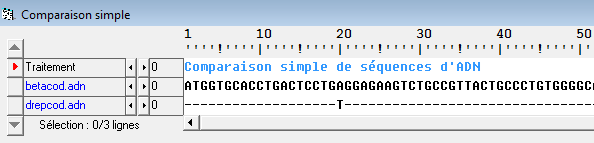
Comme on peut le voir il s’agit d’une comparaison de deux séquences. En haut, la séquence de référence, c’est l’individu témoin (allèle sauvage ou allèle sain). En dessous, c’est l’allèle de l’individu muté. On a choisi le gène qui code pour la bêta-globine, une des sous-unités de l’hémoglobine. L’hémoglobine est une molécule que l’on retrouve dans le cytoplasme des globules rouges.

Quand on compare ces deux séquences grâce au logiciel Anagène, on voit qu’il y a une seule différence dans la séquence en nucléotides des allèles étudiés. Ici, le nucléotide 20, l’adénine (A), a été substitué par le nucléotide thymine (T). C’est une mutation par substitution. Le reste de la séquence des nucléotides est rigoureusement identique entre l’allèle sain et l’allèle muté, de l’individu drépanocytaire.
II. Quelle est la conséquence de cette mutation ?
On sait qu’un triplet de nucléotides (ou codon) code pour un acide aminé. Il s’agit donc de voir si GAG et GTG (ou GUG) codent pour le même acide aminé. Puisque le code génétique est redondant, on pourrait espérer que c’est le cas. On peut alors utiliser Anagène et demander de traduire le brin d’ADN en polypeptide. La traduction par comparaison nous révèle une erreur au 6e acide aminé. Au lieu d’avoir l’acide aminé Glu (acide glutamique), il y a, dans le cas du malade, l’acide aminé Val.
(Attention : la méthionine en position 1 n’est pas comptabilisée. Elle sera lysée par une méthionine aminopeptidase.)
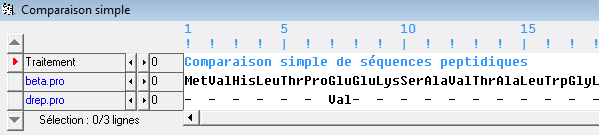
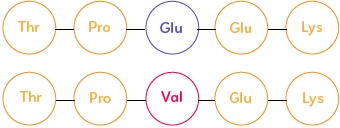
On repère les sphères qui symbolisent les acides aminés, liés par des liaisons peptidiques (noire). Le début de la séquence de nucléotides était la même donc la séquence peptidique est la même :
– Pour l’individu témoin : thréonine codé par ACT puis proline, puis acide glutamique, acide glutamique puis lysine.
– Pour l’individu drépanocytaire : le 6e acide aminé n’est pas l’acide glutamique mais la Valine. Cela est dû, en amont, à la transformation du codon GAG en GTG.
III. Cette variation dans la séquence peptidique engendre-t-elle une modification dans la structure tertiaire de la molécule ?
On sait qu’une protéine est une séquence ordonnée d’acides aminés. Cette protéine a une fonction permise par la structure tridimensionnelle ou structure tertiaire de cette protéine. Quand on se pose cette question, on peut utiliser le logiciel Rastop qui permet d’avoir une vision 3D de la protéine saine et de la protéine issue de l’individu drépanocytaire.
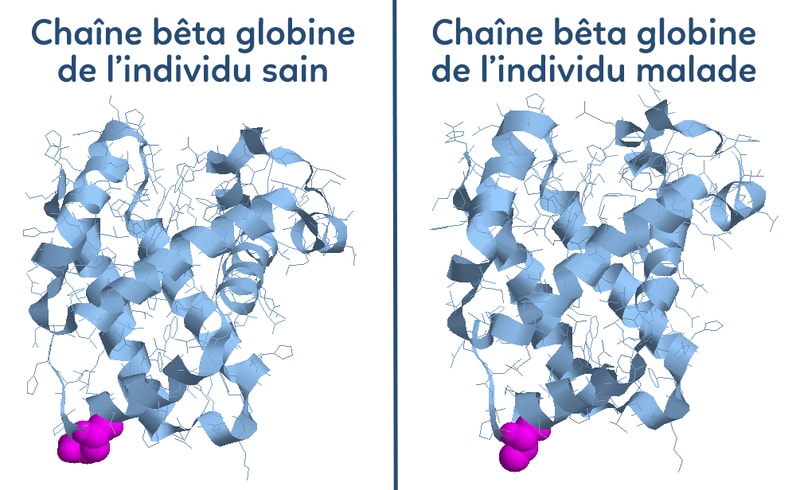
On constate qu’au niveau 3D, les deux protéines ont exactement la même forme pourtant il y a bien une mutation génétique, il y a bien une différence dans la séquence primaire du polypeptide. Si elles ont la même forme c’est qu’elles ont la même fonction : fixer de manière réversible le dioxygène. Il y a une subtilité : l’acide glutamique chez l’individu sain présente une fonction carboxyle COO– que la valine n’a pas.
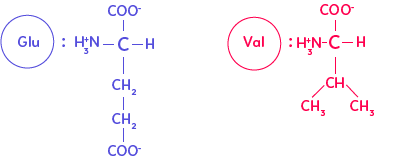
La valine est moins chargée négativement que l’acide glutamique initial. Cette charge négative qu’il y a dans la molécule saine engendre la dissolution des molécules d’hémoglobine dans le cytoplasme du globule rouge. Les charges négatives se repoussent. Alors que, chez l’individu malade, la valine, comme elle n’est pas chargée négativement, lorsque l’hémoglobine n’a pas fixé de dioxygène, les chaînes ont tendance à s’agglomérer et forment des polymères rigides : des câbles.
De sorte qu’à l’échelle cellulaire, sur un frottis sanguin chez l’individu sain, les globules rouges ont une forme bien arrondie et sont nombreux. Par contre chez l’individu malade, drépanocytaire, on voit moins de globules rouges, certains sont en faucilles (d’où l’adjectif « drépanocytaire ») ou n’ont pas de forme régulière.
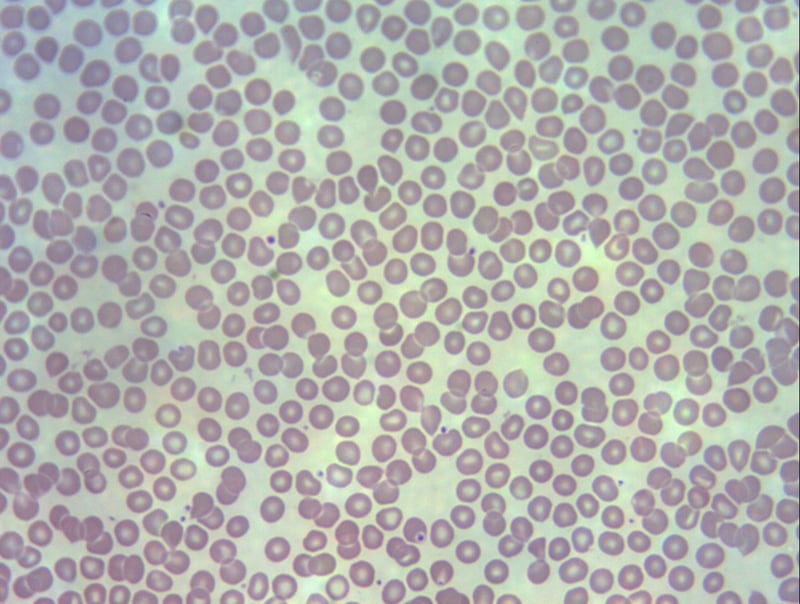
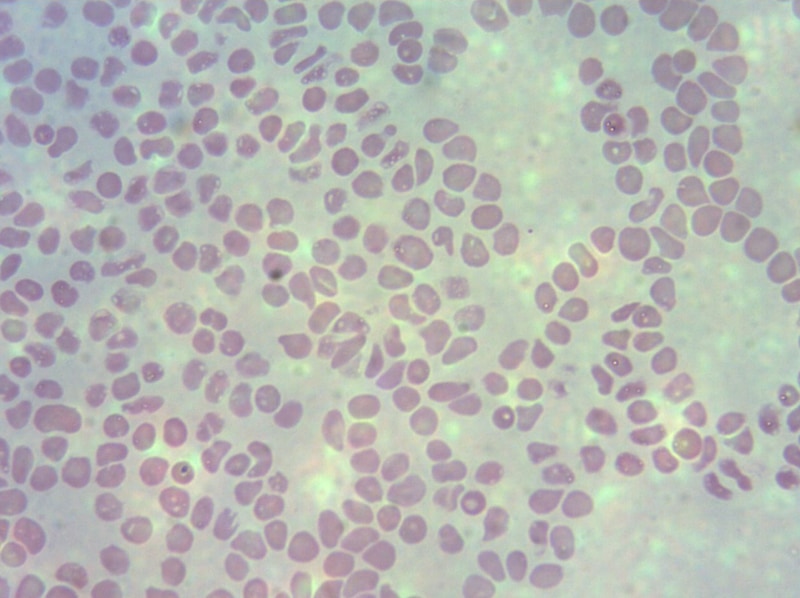
Pourquoi n’ont-ils pas de formes régulières ?
Parce que l’hémoglobine, chez un individu malade, a formé des câbles rigides qui déforment le globule rouge.
Enfin, l’échelle cellulaire a des répercussions à l’échelle macroscopique. Chez l’individu sain, les globules rouges petits, ronds, souples passent facilement dans la circulation sanguine. Chez l’individu malade, les globules rouges déformés (faucilles), cassants, ont une durée de vie courte, d’où l’anémie chez les individus malades. Et puis, il y a obstruction des vaisseaux sanguins qui peut entraîner des crises relativement douloureuses. Quand le vaisseau est très fin, on parle de capillaire, si le globule rouge qui passe est peu déformable, cela peut obstruer le capillaire et être très douloureux au moment du passage.
Altération du génome et cancérisation
Avant d’aborder les processus de cancérisation, il faut rappeler qu’une cellule dans un organisme pluricellulaire n’est pas une cellule isolée. Elle est en contact constant avec les cellules environnantes, elle appartient à un tissu et elle collabore et communique (par le biais de protéines ou de molécules de communication) avec les cellules qui sont en contact avec elle. Ces cellules de l’organisme (cellules somatiques) sont programmées pour mourir : c’est le processus apoptotique. La cellule subit un certain nombre de divisions contrôlées et elle finit par mourir. C’est le processus normal, en effet, nous sommes mortels. Seules les cellules souches ont une capacité de division mitotique « infinie » même si elles finissent elles aussi par ne plus pouvoir se diviser.
Les cellules somatiques sont donc programmées pour mourir. Quand on dit « programmé », cela signifie qu’au niveau de leur génome, il existe certains gènes qui contrôlent les divisions cellulaires, les cycles mitotiques. Ce sont des gènes suppresseurs de tumeur. Par exemple, le gène P53 ; le gène Rb (pour Rétinoblastome) et d’autres gènes appelés proto-oncogènes comme Myc et Ras qui sont là pour favoriser les divisions cellulaires. Tout est sous contrôle, les cellules somatiques sont programmées pour un certain nombre de divisions.
I. Mutations
Dans le schéma ci-dessous, on part d’un tissu avec des cellules somatiques représentées en jaune et par le biais du hasard ou sous l’influence d’un agent mutagène, une cellule représentée en violet subit une mutation. Plus précisément, son ADN subit une mutation.
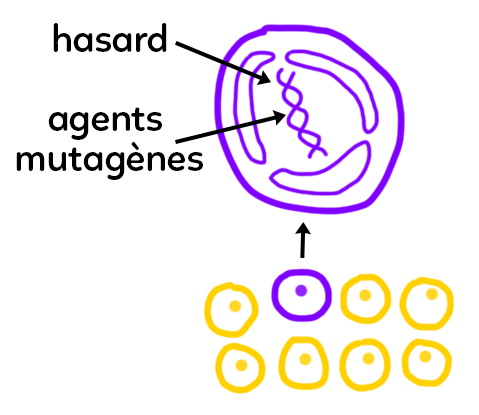
– Cela peut être dû au hasard : l’ADN est fait d’une séquence ordonnée de nucléotides faits de base azotée et il existe des formes tautomères de ces bases. Le hasard fait qu’une forme peut passer vers une autre et que lors de la réplication, il y a un processus de mutation. Mais il existe des systèmes de réparation. On considère que la mutation due au hasard a une fréquence de 10-9 ce qui est relativement rare. De plus, sur les deux mètres d’ADN et les trois giga de paires de bases, seulement 2 % sont codants.
– Cela peut être dû aux agents mutagènes comme le benzopyrène présent dans la fumé de cigarette ou de pot d’échappement. Il y a des molécules chimiques comme la riboflavine, des agents ionisants, des rayonnements UV qui peuvent induire des lésions au niveau de l’ADN ou des dimères (des ponts) au sein de deux thymines par exemple. Il y a aussi des virus comme le papillomavirus qui intervient sur la protéine P53.
II. Cancérisation
Ainsi, soit le hasard, soit des agents mutagènes provoquent des mutations sur des gènes clés des divisions cellulaires. Si la mutation arrive, cette cellule obtient la capacité de se multiplier de manière très rapide. On peut le voir phénotypiquement. En effet, normalement la cellule a une forme bien définie.
Dans ce cas elle devient souvent plus petite et a un gros noyau, elle perd sa forme initiale ce qui permet parfois en microscopie optique de déceler une cellule qui a commencé un processus de cancérisation. La cancérisation est un processus en plusieurs étapes relativement longues, en plusieurs années. Une cellule mute et va alors se multiplier de manière indéfinie et anarchique.
Une autre propriété d’une cellule cancéreuse (ou qui devient cancéreuse) est que jusqu’alors quand elle était au contact des autres cellules au sein de son tissu, il y avait un effet d’inhibition (« je suis au contact, je reconnais les autres ») donc dans l’esprit collaboratif, elle ne se multipliait pas. Quand une cellule devient cancéreuse, elle perd tout contact avec les autres cellules et elle se multiplie, il n’y a plus d’inhibition de contact. C’est le début du processus de cancérisation.
A. Tumeur primaire
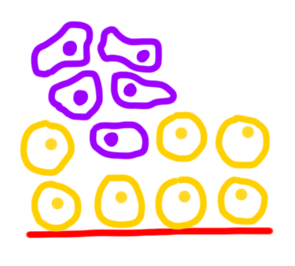
La cellule cancéreuse se multiplie en une multitude de cellules filles avec les mêmes mutations. Ces cellules filles ont la capacité de division anarchique et l’absence d’inhibition de contact. On parle alors d’une tumeur. La tumeur est un grossissement.
Dans un premier temps, elle est bégnine si les cellules ne partent pas du lieu de naissance. Une tumeur de la taille d’une tête d’épingle équivaut à 10 millions de cellules, ce qui est déjà beaucoup et rapide. Mais, il faut tout de même plusieurs années pour que cela se mette en place, on parle de tumeur primaire.
B. Tumeur secondaire
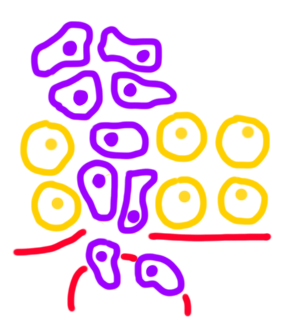
Ces cellules tumorales vont acquérir au cours du temps une dernière capacité : elles sont capables de quitter le tissu initial. Elles sont capables de lisser la lame basale et d’aller dans les vaisseaux sanguins. Une fois dedans, par le biais de la circulation sanguine, elles peuvent coloniser d’autres organes, on parle alors de tumeur secondaire. Après avoir colonisé d’autres organes et s’être multipliée, on parle alors de métastase.
Parallèlement aux autres processus et alors que certaines cellules sont parties dans la circulation sanguine, quand les métastases sont là, la tumeur continue de grossir. Quand elle atteint la taille d’une noisette, il y a environ un milliard de cellules. Le processus de cancérisation est déjà bien engagé.
L’idéal est de pouvoir identifier la tumeur avant que les métastases apparaissent, autrement dit avant que les cellules cancéreuses aient quitté leur lieu de naissance pour pouvoir, par une ablation chirurgicale, retirer cette tumeur primaire.
